离子方程式书写与正误判断的“七项 ”注意
离子反应是高中化学重要的基本概念之一 , 也是高考试题的热点题型之一 。考纲明确规定能熟练掌握离子方程 式的书写 , 并能正确判断离子方程式的正误 。由于离子反应贯穿于整个中学化学知识之中 , 内容丰富 , 知识涵量大 , 化学生的思维层次不够 , 解答往往顾此失彼 。现将离子方程式的书写、离子方程式的正误判断等两类试题的“七项”注意归纳总结如下:

文章插图
一、看离子反应是否符合客观事实 , 不可主观臆造产物及反应物 。如:
1.铁与稀硫酸反应误写成:
2Fe+6H+=Fe3++3H2↑(应该生成Fe2+)
2.铁与稀硝酸反应误写成:
Fe+2H+=Fe2++H2↑(铁与稀硝酸反应应该生成 NO和H2O , 而不放出H2)
3.四氧化三铁与稀硝酸反应误写成:
Fe3O4+8H+=Fe2++2Fe3++4H2O(稀硝酸强氧化性 , 氧化Fe2+ , 并且生成 NO和H2O)
4.氢氧化铁与过量氢碘酸反应误写成:
Fe(OH)3+3H+=Fe3++3H2O(考虑Fe3+氧化 I-生成Fe2+和 I2)
5.向次氯酸钙溶液中通入少量的二氧化硫气体误写成:
Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO(应该考虑HClO氧化CaSO3 , 生成CaSO4和 HCl)
6.向溴乙烷中滴入硝酸银溶液检验其中溴元素误写成:
Ag++Br-=AgBr↓(应该考虑溴乙烷先用NaOH水解 , 再加HNO3酸化才生成AgBr↓)
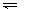
文章插图
二、看“=”“”“↓”“↑”及必要条件是否正确、齐全 。如:
1.向沸水中滴入饱和的氯化铁溶液制备氢氧化铁胶体应写作:

文章插图
Fe3++3H2O Fe(OH)3(胶体) +3H+
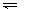
文章插图
2.单水解应写“” , ↓”“↑”如:
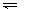
文章插图
①氯化铵溶于水应写作:NH4++ H2ONH3·H2O+ H+
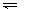
文章插图
②硫化钠的第一步水解应写作:S2-+ H2OHS-+OH-
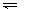
文章插图
碳酸氢钠溶于水应写作:HCO3-+H2OH2CO3+OH-
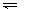
文章插图
④氯化铁溶于水应写作:Fe3++ 3H2OFe(OH)3+3H+
3.双水解应写“=”“↑”“ ↓”
如:硫酸铝溶液与小苏打溶液反应:Al3++3HCO3-=Al(OH)3↓+3CO2↑
三、看表示各物质的化学式是否正确 。如:
1.弱酸的酸式根应写作:
HCO3-、HS-、H2PO4-、HPO42-
2.强酸的酸式根HSO4-在水溶液中通常应写作H++SO42-
3.澄清石灰水 , 饱和石灰水写作:Ca2+、OH-;而石灰乳写作:Ca(OH)2 。
四、看是否漏掉离子反应 。如:
1.氢氧化钡溶液与硫酸铜溶液反应误写成:
Ba2++SO42-=BaSO4↓ , 漏掉了Cu2+与 OH-的反应 。
2.向溴化亚铁溶液中通入足量的氯气误写成:
2Fe2++Cl2 = 2Fe3++2Cl- , 漏掉了Cl2与 Br-的反应 。
(足量的氯气先氧化 Fe2+ , 再氧化 Br-生成 Fe3+和Br2)
五、看元素是否守恒、电荷是否守恒、电子是否守恒 。如:
1.钠与水反应误写成:
推荐阅读
- 叙利亚危机十周年记忆,叙利亚危机的前世今生
- 歌唱时颤音怎么唱? 怎么唱颤音
- 感恩节的来历,今天是11月24日感恩节 感恩节的由来来历习俗
- 湖北台奇妙的汉字什么时间播出
- 西游记作者是吴承恩还是李春芳,西游记的真正的作者是丘处机吗
- 3月20日支付宝蚂蚁庄园的题目答案
- 设置共享网络打印机的方法教程 如何设置网络打印机
- 2018好听的微信网名最新版! 2018年最好听的微信名
- 降落伞的原理,降落伞与火箭弹的运动竟是一回事?| 曹则贤《军事物理学》


